| Nome completo ufficiale |
Fattore inibitorio della leucemia umana ricombinante (rHuLIF) |
| sequenza |
 |
| Sequenza di aminoacidi |
SPLPITPVNA TCAIRHPCHN NLMNQIRSQL AQLNGSANAL FILYYTAQGE PFPNNLDKLC GPNVTDFPPF HANGTEKAKL VELYRIVVYL GTSLGNITRD QKILNPSALS LHSKLNATAD ILRGLLSNVL CRLCSKYHVG HVDVQFDT LKKQGKKY |
| Sinonimi |
Fattore stimolante la differenziazione, Fattore D, Inibitore LPL derivato dal melanoma, MLPLI |
| Numero di accesso |
P15018 |
| GeneID |
3976 |
| Sommario |
Il fattore inibitorio della leucemia (LIF) è un membro della famiglia dell'Interleuchina 6. Questa proteina è espressa principalmente nel trofetoderma dell'embrione in via di sviluppo, con il suo recettore LIFR espresso in tutta la massa cellulare interna. LIF ha la capacità di indurre la differenziazione terminale nelle cellule leucemiche. Le sue attività comprendono l'induzione della differenziazione ematopoietica nelle cellule leucemiche normali e mieloidi, l'induzione della differenziazione delle cellule neuronali e la stimolazione della sintesi proteica di fase acuta negli epatociti. LIF è utilizzato nella coltura di cellule staminali embrionali di topo, perché la rimozione di LIF spinge le cellule staminali verso la differenziazione, ma mantengono il loro potenziale proliferativo o pluripotenza. Viene anche utilizzato nella sperimentazione clinica di fase II, che può aiutare l'impianto di embrioni in donne che non sono riuscite a rimanere incinta nonostante le tecnologie di riproduzione assistita (ART). LIF umano maturo (180 aa) condivide l'identità di sequenza del 78 %, 82 %, 91 %, 88 % e 87 % aa con LIF di topo, ratto, cane, bovino e suino, rispettivamente. |
| Fonte |
Escherichia coli. |
| Peso molecolare |
Circa 19.7 kDa, una singola catena polipeptidica non glicosilata contenente 180 amminoacidi. |
| Attività biologica |
Completamente biologicamente attivo rispetto allo standard. La ED50 determinata dalla proliferazione dose-dipendente delle cellule TF-1 umane è inferiore a 0.1 ng/ml, corrispondente a un'attività specifica > 1.0 × 107 UI/mg. |
| Forma
|
Polvere liofilizzata bianca filtrata sterile. |
| Formulazione |
Liofilizzato da una soluzione concentrata filtrata 0.2 um in PBS, pH 7.4. |
| endotossina |
Meno di 1 EU/ug di rHuLIF come determinato dal metodo LAL. |
| Ricostituzione |
Si consiglia di centrifugare brevemente questa fiala prima dell'apertura per portare il contenuto sul fondo. Ricostituire in acqua distillata sterile o tampone acquoso contenente 0.1 % BSA a una concentrazione di 0.1-0.2 mg/mL. Le soluzioni madre devono essere suddivise in aliquote di lavoro e conservate a ≤ -20 °C. Ulteriori diluizioni devono essere effettuate in appropriate soluzioni tamponate. |
| Stabilità e conservazione |
Utilizzare un congelatore a sbrinamento manuale ed evitare ripetuti cicli di congelamento-scongelamento.- 12 mesi dalla data di ricevimento, da -20 a -70 °C come fornito.- 1 mese, da 2 a 8 °C in condizioni sterili dopo la ricostituzione.- 3 mesi, Da -20 a -70 °C in condizioni sterili dopo la ricostituzione. |
| Riferimenti |
|
| PAGINA SDS |
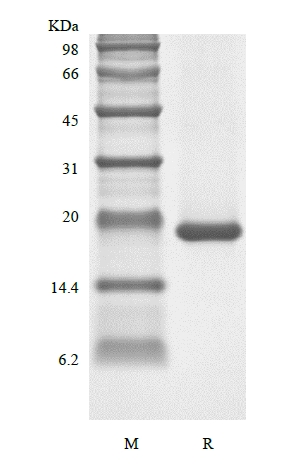 |
| Download della scheda di dati di sicurezza (SDS) |
Clicca per scaricare |
| Download della scheda tecnica (TDS) |
Clicca per scaricare |



