| Nome completo ufficiale |
Fattore di crescita epidermico umano ricombinante (rHuEGF) |
| sequenza |
 |
| Sequenza di aminoacidi |
NSDSECPLSH DGYCLHDGVC MYIEALDKYA CNCVVGYIGE RCQYRDLKWW ELR |
| Sinonimi |
Urogastrone, URG |
| Numero di accesso |
P01133 |
| GeneID |
|
| Sommario |
Il fattore di crescita epidermico (EGF) è stato originariamente scoperto in preparazioni grezze di fattore di crescita nervoso preparato dalle ghiandole sottomascellari di topo come attività che induceva l'apertura precoce delle palpebre, l'eruzione degli incisivi, l'inibizione della crescita dei capelli e l'arresto della crescita quando iniettati nei topi neonati. L'EGF umano è stato isolato dall'urina in base al suo effetto inibitorio sulla secrezione gastrica e di conseguenza chiamato urogastrone. L'EGF è il prototipo di una famiglia di fattori di crescita derivati da precursori ancorati alla membrana. Tutti i membri di questa famiglia sono caratterizzati dalla presenza di almeno un'unità strutturale EGF (definita dalla presenza di un motivo conservato a 6 cisteine che forma tre legami disolfuro) nel loro dominio extracellulare. L'EGF è inizialmente sintetizzato come una proteina transmembrana precursore di 130 kDa contenente 9 unità EGF. La sequenza EGF solubile matura corrisponde all'unità EGF situata prossimalmente al dominio transmembrana. Il precursore dell'EGF di membrana è in grado di legarsi al recettore dell'EGF ed è stato segnalato come biologicamente attivo. L'EGF umano maturo condivide il 70% dell'identità di sequenza aa con l'EGF maturo di topo e ratto. |
| Fonte |
Escherichia coli. |
| Peso molecolare |
Circa 6.2 kDa, una singola catena polipeptidica non glicosilata contenente 53 amminoacidi. |
| Attività biologica |
Completamente biologicamente attivo rispetto allo standard. L'ED50 come determinato da un saggio di proliferazione cellulare utilizzando cellule Balb/c 3T3 murine è inferiore a 1 ng/ml, corrispondente a un'attività specifica > 1.0 × 106 UI/mg. |
| Forma
|
Polvere liofilizzata bianca filtrata sterile. |
| Formulazione |
Liofilizzato da una soluzione concentrata filtrata 0.2 um in PBS, pH 7.4. |
| endotossina |
Meno di 1 EU/ug di rHuEGF come determinato dal metodo LAL. |
| Ricostituzione |
Si consiglia di centrifugare brevemente questa fiala prima dell'apertura per portare il contenuto sul fondo. Ricostituire in acqua distillata sterile o tampone acquoso contenente 0.1 % BSA a una concentrazione di 0.1-1.0 mg/mL. Le soluzioni madre devono essere suddivise in aliquote di lavoro e conservate a ≤ -20 °C. Ulteriori diluizioni devono essere effettuate in appropriate soluzioni tamponate. |
| Stabilità e conservazione |
Utilizzare un congelatore a sbrinamento manuale ed evitare ripetuti cicli di congelamento-scongelamento.- 12 mesi dalla data di ricevimento, da -20 a -70 °C come fornito.- 1 mese, da 2 a 8 °C in condizioni sterili dopo la ricostituzione.- 3 mesi, Da -20 a -70 °C in condizioni sterili dopo la ricostituzione. |
| Riferimenti |
|
| PAGINA SDS |
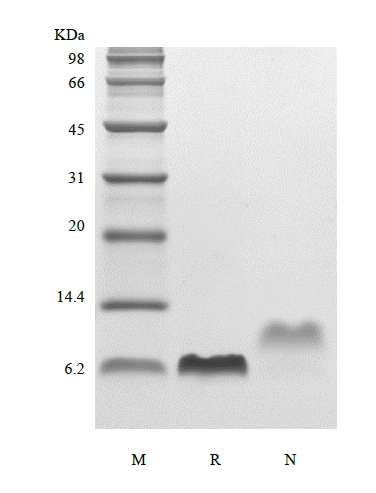 |
| Download della scheda di dati di sicurezza (SDS) |
Clicca per scaricare |
| Download della scheda tecnica (TDS) |
Clicca per scaricare |



